Όροι και προϋποθέσεις λειτουργίας του Εθνικού Οργανισμού Επαλήθευσης Φαρμάκων (NMVO)
Εισαγωγή στο ευρωπαϊκό σύστημα επαλήθευσης των φαρμάκων (EMVS)
Στις 9 Φεβρουαρίου 2019 τίθεται σε εφαρμογή ο νέος κανονισμός που θα ισχύσει στη Ευρωπαϊκή Ένωση (ΕΕ) με πολύ σημαντικές αλλαγές για την ασφάλεια των ασθενών και την διακίνηση των φαρμάκων.
Προκειμένου να αντιμετωπιστεί η απειλή της εισόδου των ψευδεπίγραφων φαρμάκων στη νόμιμη αλυσίδα εφοδιασμού, το Ευρωπαϊκό Κοινοβούλιο και το Συμβούλιο εξέδωσαν κανονισμό σχετικά με τα ψευδεπίγραφα φάρμακα (2011/62 / ΕΕ) (για την τροποποίηση της οδηγίας 2001/83 / ΕΚ). Στόχος του είναι η βελτίωση της ασφάλειας των ασθενών με την ανάθεση εντολής στους Κατόχους Αδειών Κυκλοφορίας (ΚΑΚ) και στους κατασκευαστές να θέσουν σε εφαρμογή ένα σύστημα το οποίο εμποδίζει την εισαγωγή ψευδεπίγραφων φαρμάκων στη νόμιμη αλυσίδα εφοδιασμού, το Ευρωπαϊκό Σύστημα Επαλήθευσης Φαρμάκων (EMVS). Το EMVS θα πρέπει να εγγυάται την αυθεντικότητα των φαρμάκων μέσω επαλήθευσης από άκρο σε άκρο.
Η επαλήθευση από άκρο σε άκρο είναι ένα σύστημα ελέγχου ταυτότητας φαρμάκων που περιλαμβάνει τα υποχρεωτικά χαρακτηριστικά ασφαλείας και ένα αποθετήριο που αποθηκεύει πληροφορίες για κάθε μεμονωμένη συσκευασία.
Οι ΚΑΚ, οι κατασκευαστές, οι χονδρέμποροι και όσοι προμηθεύουν φάρμακα στο κοινό θα πρέπει να σαρώνουν τα φάρμακα σε διάφορα σημεία της αλυσίδας εφοδιασμού για να τα εισαγάγουν στο αποθετήριο, να ελέγξουν την αυθεντικότητά τους και να τα αποσύρουν από τη βάση δεδομένων τη στιγμή της διανομής.
Μεταφόρτωση: Ευρωπαϊκό επίπεδο
Οι κατασκευαστές μπορούν να φορτώσουν τα μοναδικά αναγνωριστικά στοιχεία μέσω του ευρωπαϊκού διανομέα (hub) και η επαλήθευση των φαρμάκων θα πραγματοποιηθεί στα εθνικά συστήματα επαλήθευσης των φαρμάκων. Τα συνολικά τεχνικά και ποιοτικά πρότυπα, όπως η διαλειτουργικότητα του συστήματος, η ιδιοκτησία δεδομένων και η πρόσβαση, συμφωνήθηκαν από τους ενδιαφερόμενους φορείς βάσει αρχών αμοιβαία επικυρωμένων που είναι συμβατές με τις απαιτήσεις του FMD.
Τα προϊόντα που εμπίπτουν στο πεδίο εφαρμογής του FMD είναι γενικά όλα τα προϊόντα που χορηγούνται με ιατρική συνταγή, με λίγες εξαιρέσεις, όπως ορίζονται στον κανονισμό (EU) 2016/161. Ενώ τα προϊόντα που δεν καλύπτονται από ιατρική συνταγή δεν εμπίπτουν σε μεγάλο βαθμό, υπάρχουν μερικές εξαιρέσεις και μπορούν να οριστούν από τις αρμόδιες εθνικές αρχές ανά αγορά.
Σημείο εξακρίβωσης φαρμάκων
Κατ’ ‘ουσία, οι κατασκευαστές θα πρέπει να εκτυπώσουν έναν κώδικα δεδομένων Matrix, ο οποίος ενσωματώνει ένα μοναδικό αναγνωριστικό (UI) και εφαρμόζει μια συσκευή κατά της παραβίασης στην εξωτερική συσκευασία όλων των φαρμάκων για κάθε μεμονωμένη συσκευασία πώλησης. Στο σημείο χορήγησης, το φάρμακο θα σαρωθεί, θα ελεγχθεί και θα επαληθευτεί ως προς την αυθεντικότητα έναντι ενός εθνικού (ή υπερεθνικού) αποθετηρίου. Εάν το μοναδικό αναγνωριστικό της συσκευασίας ταιριάζει με τις πληροφορίες του αποθετηρίου, το πακέτο αποσύρεται και παρέχεται στον ασθενή. Διαφορετικά, εάν υπάρχει προειδοποίηση σχετικά με αυτό το πακέτο, τότε το σύστημα θα τονίσει αυτό ως ένα εξαιρετικό συμβάν και η συσκευασία δεν θα παραδοθεί στον ασθενή. Πρέπει να διερευνηθεί εάν το πακέτο έχει παραποιηθεί ή όχι.


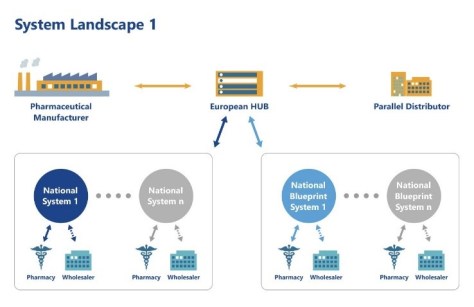
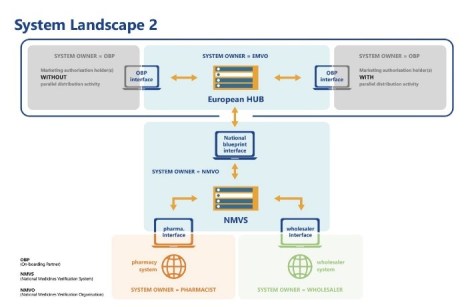
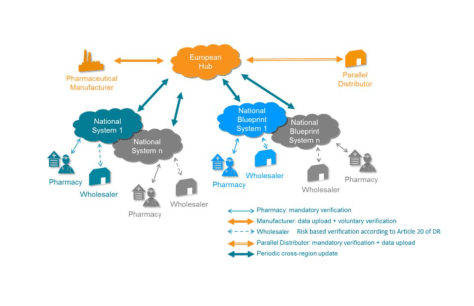
Πηγή: EMVO 2019
«Κάθε ευρωπαϊκή χώρα πρέπει να εφαρμόσει ένα Εθνικό Σύστημα Επαλήθευσης Φαρμάκων»
Εισαγωγή στις εθνικές αρμοδιότητες
Αναφορικά με τον κατ ‘εξουσιοδότηση κανονισμό (ΕΕ) 2016/161 στο άρθρο του 32, η Ευρωπαϊκή Επιτροπή αναφέρει τη δομή που θα πρέπει να υιοθετήσει το σύστημα των αποθετηρίων. Έτσι, θα αποτελείται από κεντρικό δρομολογητή πληροφοριών και δεδομένων (ο ευρωπαϊκός κεντρικός σταθμός) και τ’αποθετήρια που εξυπηρετούν την επικράτεια ενός ή πολλαπλών κρατών μελών. Αυτά τα αποθετήρια θα πρέπει όλα να συνδεθούν με το EU-Hub.
Ως εκ τούτου, κάθε ευρωπαϊκή χώρα (της Ευρωπαϊκής Ένωσης, του Ευρωπαϊκού Οικονομικού Χώρου και της Ελβετίας) πρέπει να εφαρμόσει ένα Εθνικό Σύστημα Επαλήθευσης των Φαρμάκων (NMVS) το οποίο θα συσταθεί και θα διαχειρίζεται ένας Εθνικός Οργανισμός Επαλήθευσης Φαρμάκων (NMVO).
Ο κύριος σκοπός του NMVS είναι να χρησιμεύσει ως πλατφόρμα επαλήθευσης ότι τα φαρμακεία ή τ’ άλλα εγγεγραμμένα μέρη – όπως οι χονδρέμποροι, οι αυτοεξυπηρετούμενοι γιατροί ή τα νοσοκομεία – θα την χρησιμοποιήσουν για να ελέγξουν την αυθεντικότητα ενός προϊόντος.
Οι κύριοι στόχοι ενός NMVS:
• Διατήρηση των σχετικών στοιχείων σειριοποίησης προϊόντων για την εθνική αγορά.
• Λήψη αναθεωρημένων / νέων δεδομένων σειριοποίησης προϊόντων από το EU-Hub.
• Εξυπηρέτηση ως πλατφόρμα επαλήθευσης για τα φαρμακεία ή άλλα εγγεγραμμένα μέρη όπως οι χονδρέμποροι και τα νοσοκομεία για να πιστοποιήσουν την αυθεντικότητα ενός προϊόντος.
• Η εξυπηρέτηση ως πλατφόρμα για τους χονδρεμπόρους στην περίπτωση εφαρμογής από το κράτος μέλος του άρθρου 23 του κανονισμού, για να επισημαίνεται μια συσκευασία προϊόντος ως ακυρωμένη πριν αυτή παραδοθεί στον ασθενή.
• Εξυπηρέτηση ως πλατφόρμα για τους χονδρεμπόρους να επισημάνουν μια συσκευασία προϊόντων ως «παροπλισμένη» π.χ. «Εξάγονται εκτός ΕΕ»
Επισκόπηση σύνδεσης NMVS
Για την εφαρμογή του EMVS, όλα τα NMVS πρέπει να συνδεθούν με το ευρωπαϊκό Hub. Πρέπει να λαμβάνονται υπόψη πολλές διατυπώσεις. συμπεριλαμβανομένης της αξιολόγησης του συστήματος, των στόχων διασφάλισης της ποιότητας και των τεχνικών απαιτήσεων.
Ίδρυση NMVOs
Εκτός από την υπογραφή της υποχρεωτικής Συμφωνίας Συμμετοχής με τον EMVO, οι Συνεργάτες / ΚΑΚ καλούνται να συνάψουν σύμβαση σε εθνικό επίπεδο και να καταβάλλουν ετήσια αμοιβή. Το ισχύον μοντέλο αμοιβής εξαρτάται από τον κάθε NMVO.
Η σύσταση και λειτουργία του ελληνικού NMVO, πρέπει να γίνει όσο το δυνατόν πιο σύντομα για να αποφασιστεί ποιος από τους πέντε end-to-end εταίρους θα καταβάλει το κόστος και σε ποιο ποσοστό για τα διαφορετικά στάδια της εφοδιαστικής αλυσίδας. Όπως έχει όμως αναγραφεί και σε πρόσφατο άρθρο άπαντα είναι κοστολογημένα, διάφανα και ευδιάκριτα. Τα κόστη που είχαν παρουσιαστεί στους εταίρους τα προηγούμενα χρόνια ήταν υπερβολικά υψηλά και αποθάρρυναν τους εταίρους του ελληνικού NMVO να προχωρήσουν στην ίδρυση του. Πρέπει ο ελληνικός NMVO να μπορεί να εξυπηρετήσει τις ευρωπαϊκές αλλά και τις ελληνικές ιδιαιτερότητες των μικρών και πολλών εξαγωγών σε άλλες χώρες. Το ίδιο και τα πληροφοριακά συστήματα που εγκαθιστούν οι φαρμακοβιομηχανίες τα οποία αναφέρονται κυρίως στην ευρωπαϊκή αγορά και όχι στη παγκόσμια αγορά η οποία θα εφαρμόσει τη σχετική οδηγία μαζί με τις δικές της απαιτήσεις για την διασφάλιση της εφοδιαστικής αλυσίδας και των ασθενών.
Συσκευασία και διακίνηση φαρμάκων. Τι αλλάζει σε 100 ημέρες.
ΕΥΔΙΑΚΡΙΤΑ ΠΛΕΟΝ ΤΑ ΚΟΣΤΗ ΣΤΟΥΣ NMVO
Προβληματισμοί γύρω από τον κανονισμό για τα ψευδεπίγραφα φάρμακα και την λειτουργία του NMVO.
Η ανάγκη ίδρυσης ενός Εθνικού Οργανισμού Επαλήθευσης Φαρμάκων (NMVO). στην Ελλάδα
Serialisation: Σχέσεις CMOs και επωνύμων εταιρειών. Τι πρέπει να γίνει.
Η ελληνική φαρμακοβιομηχανία σε κρίσιμο σταυροδρόμι. Προκλήσεις και εμπόδια.
ΨΕΥΔΕΠΙΓΡΑΦΑ ΦΑΡΜΑΚΑ ΚΑΙ ΕΛΛΗΝΙΚΗ ΠΡΑΓΜΑΤΙΚΟΤΗΤΑ